Científicos de la Universidad Northwestern han desarrollado un nuevo material
bioactivo que regeneró con éxito cartílago de alta calidad en las articulaciones de
la rodilla de un modelo animal grande, según los resultados publicados en las
Actas de la Academia Nacional de Ciencias.
Samuel Stupp, PhD, Profesor del Consejo de Administración de Ciencia e
Ingeniería de Materiales, Química, Medicina e Ingeniería Biomédica y director del
Instituto Simpson Querrey de BioNanotecnología.
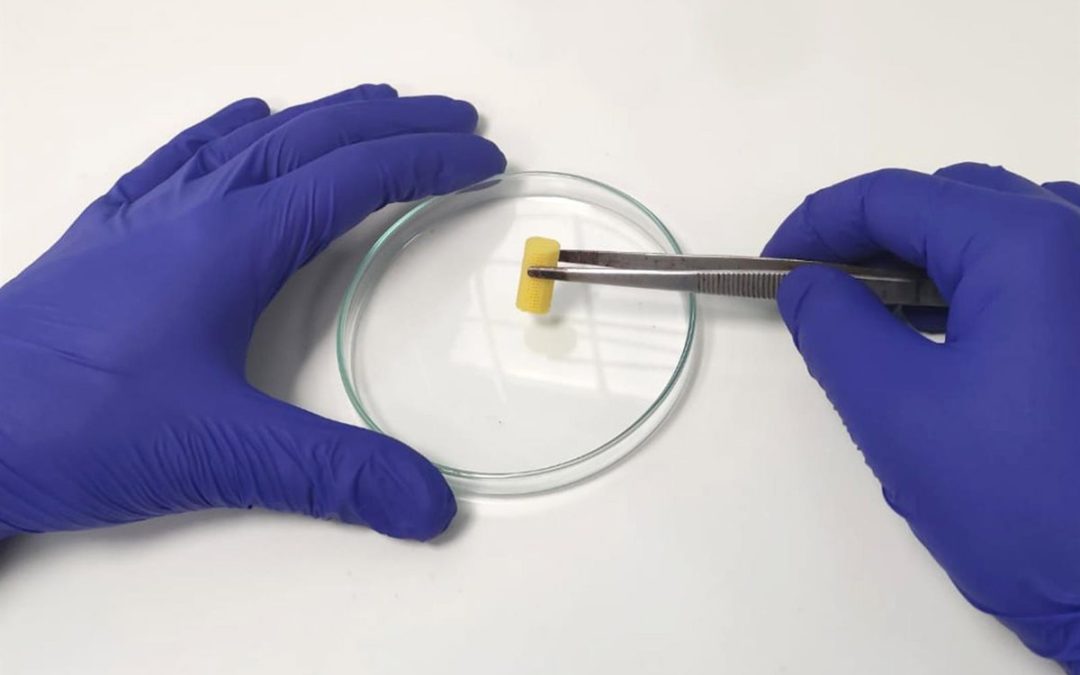
Aunque parece una sustancia gomosa, el material es en realidad una red compleja
de componentes moleculares que trabajan juntos para imitar el entorno natural del
cartílago en el cuerpo. En el nuevo estudio, los científicos aplicaron el material al
cartílago dañado de las articulaciones de las rodillas de los animales. En tan solo
seis meses, los autores observaron evidencia de una mejor reparación, incluyendo
el crecimiento de cartílago nuevo que contiene biopolímeros naturales (colágeno II
y proteoglicanos), que permiten una resiliencia mecánica indolora en las
articulaciones. Los científicos dicen que con más trabajo, el nuevo material podría
potencialmente algún día usarse para prevenir cirugías de reemplazo total de
rodilla, tratar enfermedades degenerativas como la osteoartritis y reparar lesiones
relacionadas con el deporte como desgarros del ligamento cruzado anterior (LCA).
“El cartílago es un componente fundamental de nuestras articulaciones”, afirmó el
Dr. Samuel Stupp, de Northwestern , quien dirigió el estudio. “Cuando el cartílago
se daña o se deteriora con el tiempo, puede tener un gran impacto en la salud
general y la movilidad de las personas. El problema radica en que, en los adultos,
el cartílago no tiene una capacidad innata para sanar. Nuestra nueva terapia
puede inducir la reparación en un tejido que no se regenera de forma natural.
Creemos que nuestro tratamiento podría ayudar a abordar una necesidad clínica
grave e insatisfecha”. Pionero de la nanomedicina regenerativa, Stupp es profesor
titular de Ciencia e Ingeniería de Materiales, Química, Medicina e Ingeniería
Biomédica en la Universidad Northwestern, donde es director fundador del Instituto
Simpson Querrey de BioNanotecnología y su centro afiliado, el Centro de
Nanomedicina Regenerativa . Stupp ocupa puestos en la Facultad de Medicina
Feinberg de la Universidad Northwestern , la Facultad de Ingeniería
McCormick y el Colegio de Artes y Ciencias Weinberg ; Jacob Lewis, exestudiante
de doctorado en el laboratorio de Stupp, es el primer autor del artículo.
¿Qué hay en el material?
El nuevo estudio surge de un trabajo publicado recientemente por el laboratorio de
Stupp, en el que el equipo utilizó “moléculas danzantes” para activar células de
cartílago humano y así impulsar la producción de proteínas que forman la matriz
tisular. En lugar de utilizar moléculas danzantes, el nuevo estudio evalúa un
biomaterial híbrido también desarrollado en el laboratorio de Stupp. El nuevo
biomaterial consta de dos componentes: un péptido bioactivo que se une al factor
de crecimiento transformante beta-1 (TGFb-1), una proteína esencial para el
crecimiento y el mantenimiento del cartílago, y ácido hialurónico modificado, un
polisacárido natural presente en el cartílago y el líquido sinovial lubricante de las
articulaciones. “Mucha gente conoce el ácido hialurónico porque es un ingrediente
popular en productos para el cuidado de la piel”, dijo Stupp. “También se
encuentra de forma natural en muchos tejidos del cuerpo humano, incluyendo las
articulaciones y el cerebro. Lo elegimos porque se asemeja a los polímeros
naturales del cartílago”. El equipo de Stupp integró el péptido bioactivo y partículas
de ácido hialurónico modificadas químicamente para impulsar la autoorganización
de fibras nanométricas en haces que imitan la arquitectura natural del cartílago. El
objetivo era crear un andamiaje atractivo para que las propias células del cuerpo
regeneraran el tejido cartilaginoso. Mediante señales bioactivas en las fibras
nanométricas, el material promueve la reparación del cartílago por parte de las
células que pueblan el andamiaje.
Clínicamente relevante para los humanos
Para evaluar la eficacia del material en la promoción del crecimiento del cartílago,
los investigadores lo probaron en ovejas con defectos de cartílago en la
articulación de la rodilla, una articulación compleja de las extremidades posteriores
similar a la rodilla humana. Este trabajo se llevó a cabo en el laboratorio de Mark
Markel, de la Facultad de Medicina Veterinaria de la Universidad de Wisconsin-
Madison. Según Stupp, las pruebas en un modelo ovino fueron vitales. Al igual
que en los humanos, el cartílago ovino es resistente y extremadamente difícil de
regenerar. Las rodillas de las ovejas y las de los humanos también presentan
similitudes en cuanto a la capacidad de carga, el tamaño y las cargas mecánicas.
“Un estudio con un modelo ovino predice mejor la eficacia del tratamiento en
humanos”, afirmó Stupp. “En otros animales más pequeños, la regeneración del
cartílago es mucho más rápida”. En el estudio, los investigadores inyectaron el
material espeso y pastoso en defectos de cartílago, donde se transformó en una
matriz gomosa. No solo se generó cartílago nuevo para rellenar el defecto a
medida que el andamio se degradaba, sino que el tejido reparado fue
consistentemente de mayor calidad en comparación con el control.
Una solución duradera
En el futuro, Stupp imagina que el nuevo material podría aplicarse a las
articulaciones durante cirugías abiertas o artroscópicas. El tratamiento estándar
actual es la cirugía de microfracturas, en la que los cirujanos crean pequeñas
fracturas en el hueso subyacente para inducir el crecimiento de nuevo cartílago.
“El principal problema del enfoque de microfractura es que a menudo resulta en la
formación de fibrocartílago (el mismo cartílago presente en nuestras orejas) en
lugar de cartílago hialino, que es el que necesitamos para tener articulaciones
funcionales”, afirmó Stupp. “Al regenerar el cartílago hialino, nuestro enfoque
debería ser más resistente al desgaste, solucionando el problema de la movilidad
reducida y el dolor articular a largo plazo, a la vez que evita la necesidad de
reconstruir las articulaciones con grandes piezas de prótesis”. El estudio fue
financiado por el Fondo Familiar Mike y Mary Sue Shannon para Sistemas de
Materiales Bioinspirados y Bioactivos para la Regeneración Musculoesquelética.